【必見!】アミノ酸の構造や種類や特性について簡単に解説してみた!

こんにちは!
私は平成生まれの管理栄養士です!
今回の記事は、たんぱく質を構成するアミノ酸について詳しく解説した記事です!
アミノ酸という言葉はもうおなじみだと思いますが、実際に詳しくはわからない・・・
そんな方のためにアミノ酸についてできる詳しく丁寧に解説していきたいと思います!
この記事を読めばあなたもアミノ酸マスター!!
たんぱく質はアミノ酸で出来ている!
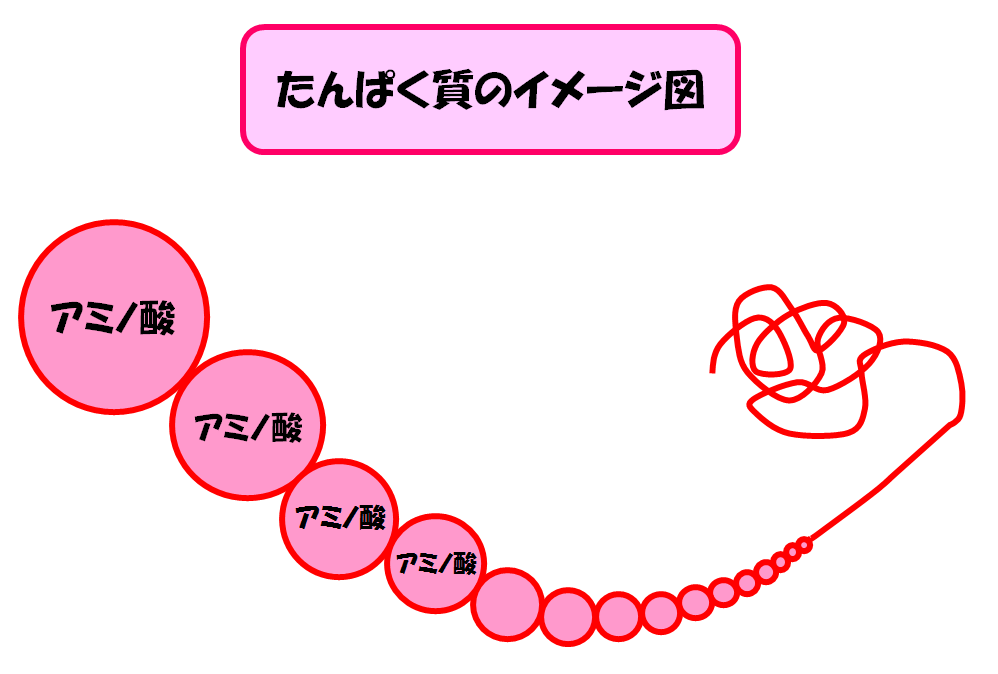
たんぱく質はアミノ酸が鎖のようにつながってできています。
たんぱく質は立体構造といって、一本の鎖がぐしゃぐしゃと立体的に絡み合って構成されています。
少しイメージしやすいようにこんな図を用意しました。

すごい適当な図ですが、たんぱく質は実際にこのようにぐしゃぐしゃとアミノ酸の鎖が絡み合っているのです。
もちろんたんぱく質はその種類によって、たんぱく質の大きさ(分子量)や構造、アミノ酸の並び方は違います。
あくまでこの図はたんぱく質の構造を理解するための図になります。
そして、そのたんぱく質の立体構造を崩していくと次の図のように一本の鎖のようになります。
一本の鎖を拡大すると、このようにアミノ酸同士が結合しているのです。
つまりたんぱく質というのは、たくさんのアミノ酸同士が結合することで長い鎖ができ、その鎖がぐしゃぐしゃと立体構造を作ってできているということです。
たんぱく質がアミノ酸でできているということの意味がなんとなくイメージできたでしょうか。
アミノ酸の構造
たんぱく質がアミノ酸によって構成されているということや、たんぱく質を構成する最小単位の物質がアミノ酸であるということはわかったと思います。
ここではそんなたんぱく質を構成するアミノ酸の構造について少し解説したいと思います。
アミノ酸の構造を理解する上ではこの図は非常に大切になります!
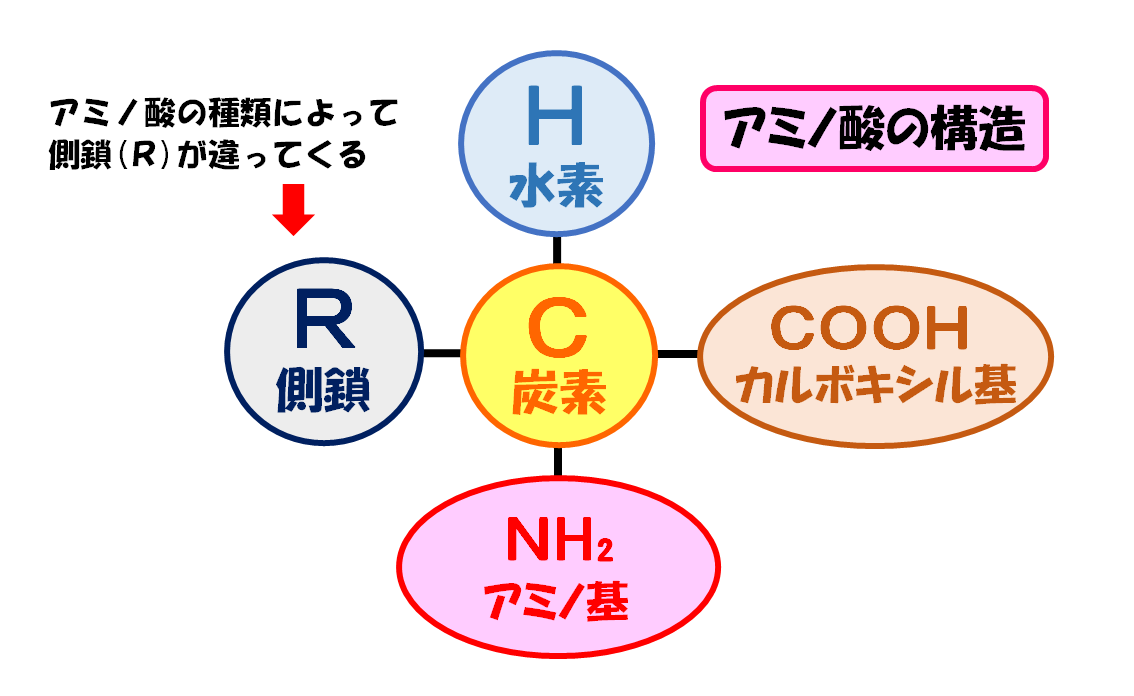
アミノ酸というのは、塩基性のアミノ基(-NH₂)と酸性のカルボキシル基(-COOH)の両方を1分子中にもつ有機化合物を言います。
真ん中の炭素(C)を中心に4本手が伸びそれぞれにアミノ基(-NH₂)、カルボキシル基(-COOH)、水素(H)、側鎖(R)が結合しているのが分かると思います。
塩基性とか酸性とかは特に覚えなくで大丈夫ですので、アミノ基(-NH₂)、カルボキシル基(-COOH)というのは覚えてほしいと思います。
アミノ酸は全て、この側鎖(R)以外の形は同じです。
この側鎖(R)の部分にどのようなものが結合しているのかでそのアミノ酸の特徴や種類が変わってくるのです!
- アミノ酸は、炭素(C)を中心に、アミノ基(-NH₂)、カルボキシル基(-COOH)、水素(H)、側鎖(R)がそれぞれ結合している
- 側鎖(R)以外のアミノ基(-NH₂)、カルボキシル基(-COOH)、水素(H)はどのアミノ酸にも共通していて、側鎖(R)の部分によってその特徴や種類が変わる
このように覚えてください!
アミノ酸の特性
アミノ酸の構造のところでも説明しましたが、アミノ酸には塩基性のアミノ基(-NH₂)と酸性のカルボキシル基(-COOH)が1つの分子中に存在しています。
そのような構造をとっているため、アミノ酸は塩基と酸の両方の性質を示す両性電解質なのです。
簡単に言うと、酸性にも塩基性にもなり得る特徴を持っているということになります。
アミノ酸は水に溶けると水中でイオン化して、中性付近では-NH₃⁺と-COO⁻と、このように解離してい両性イオンになります。
水中でイオン化したそれぞれのアミノ酸は、ある一定の㏗になった時に、-NH₃⁺と-COO⁻のが同じ数になります。
この各アミノ酸に存在する-NH₃⁺と-COO⁻が同じ数になる一定の㏗を等電点と言います。
水中に存在するイオン⁺と⁻の数が一致する㏗を等電点と呼ぶのですが、栄養学では等電点はあまり出てこないので特に覚える必要性はありません。
しかしこの等電点というものを利用して、乳からチーズを作ったり食品の化学には非常に大事な概念になります!
たんぱく質を構成するアミノ酸の種類
アミノ酸の構造がなんとなく理解できたら次はたんぱく質を構成するアミノ酸の種類について解説していきます。
たんぱく質を構成するアミノ酸は全部で20種類です。
たんぱく質の種類によってその分子量はとても大きくなりますが、それでもそんな大きなたんぱく質を構成するアミノ酸の種類も変わらず20種類しかありません。
その20種類のアミノ酸が様々な配列や並び方をすることで一本の鎖を作り、それが立体構造をとってたんぱく質になるのです。
それではその20種類のアミノ酸を紹介します。
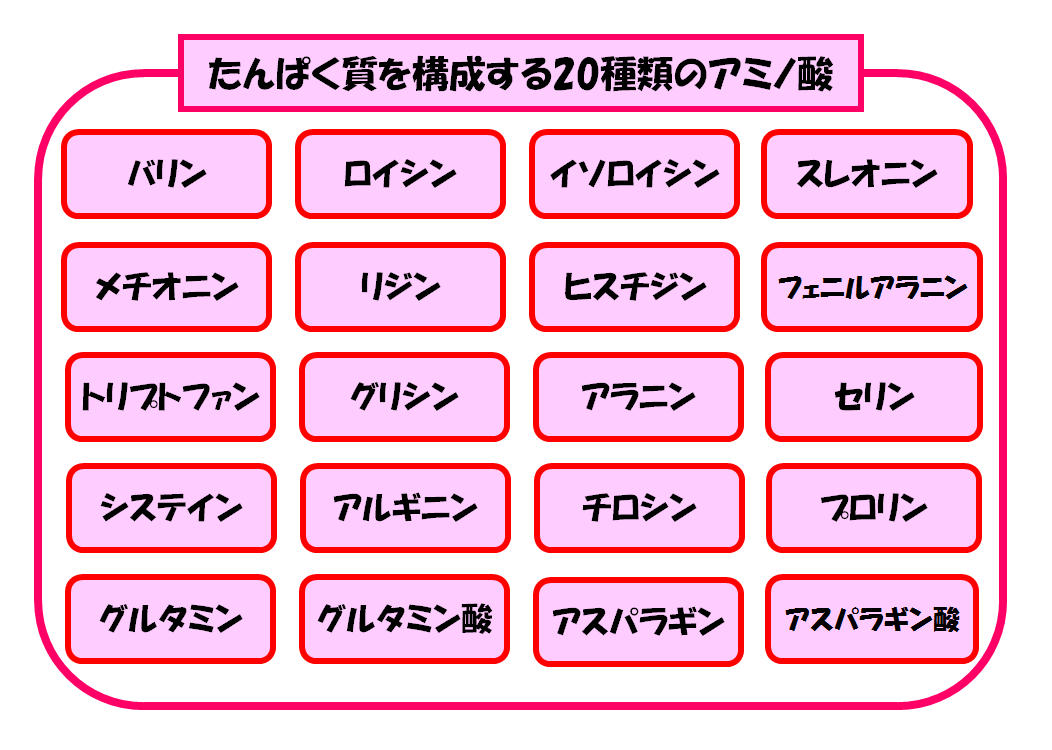
上の図に書かれている20種類のアミノ酸がたんぱく質を構成しています。
そしてこれらの20種類のアミノ酸たちは、側鎖(R)にどのようなものが結合しているのかが違うのです。

この上の図の側鎖(R)の部分を赤い点線が囲みながらそれぞれのアミノ酸の構造や特徴を見ていきたいと思います!
グリシン
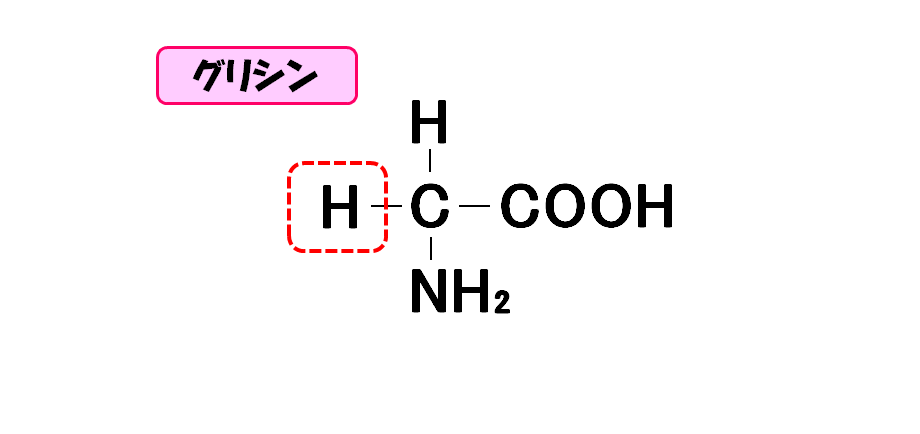
- 3文字略記号・・・Gly
- 1文字略記号・・・G
- 分子量・・・75.1
- 等電点・・・5.97
アラニン
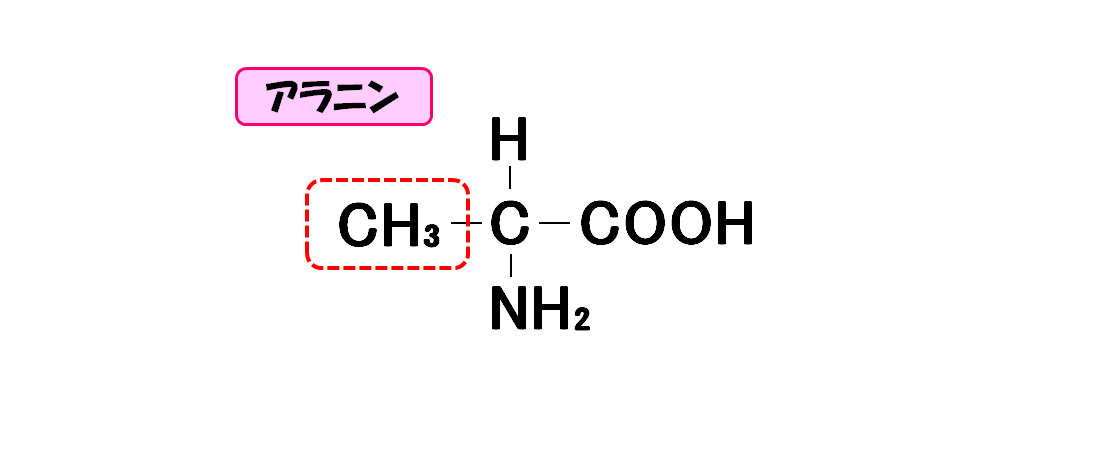
- 3文字略記号・・・Ala
- 1文字略記号・・・A
- 分子量・・・89.1
- 等電点・・・6.02
バリン
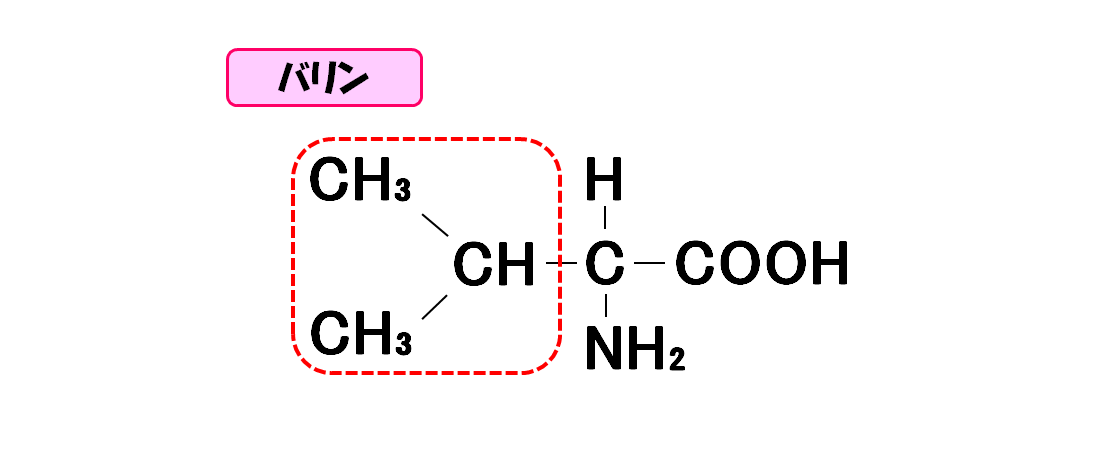
- 3文字略記号・・・Val
- 1文字略記号・・・V
- 分子量・・・117.1
- 等電点・・・5.97
ロイシン
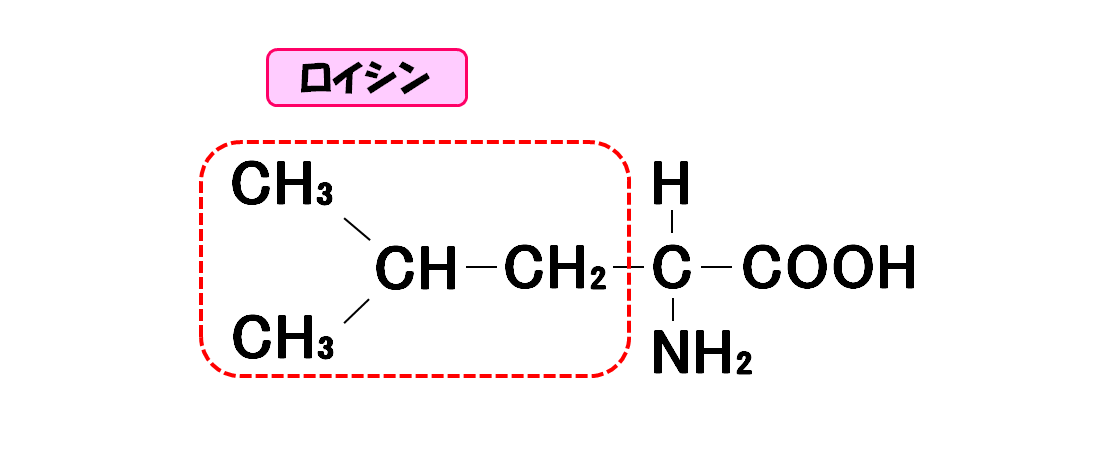
- 3文字略記号・・・Leu
- 1文字略記号・・・L
- 分子量・・・131.2
- 等電点・・・5.98
イソロイシン

- 3文字略記号・・・Ile
- 1文字略記号・・・I
- 分子量・・・131.2
- 等電点・・・6.02
セリン
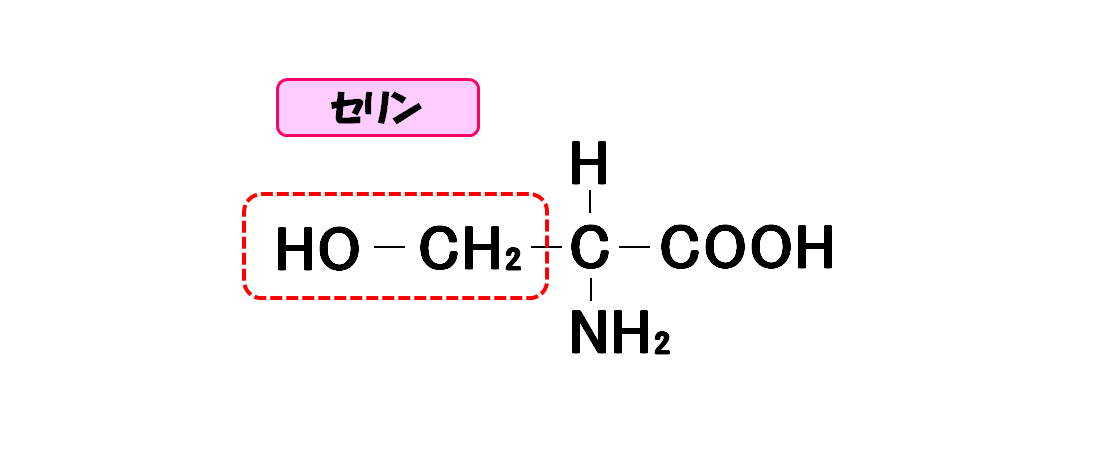
- 3文字略記号・・・Ser
- 1文字略記号・・・S
- 分子量・・・105.1
- 等電点・・・5.68
スレオニン
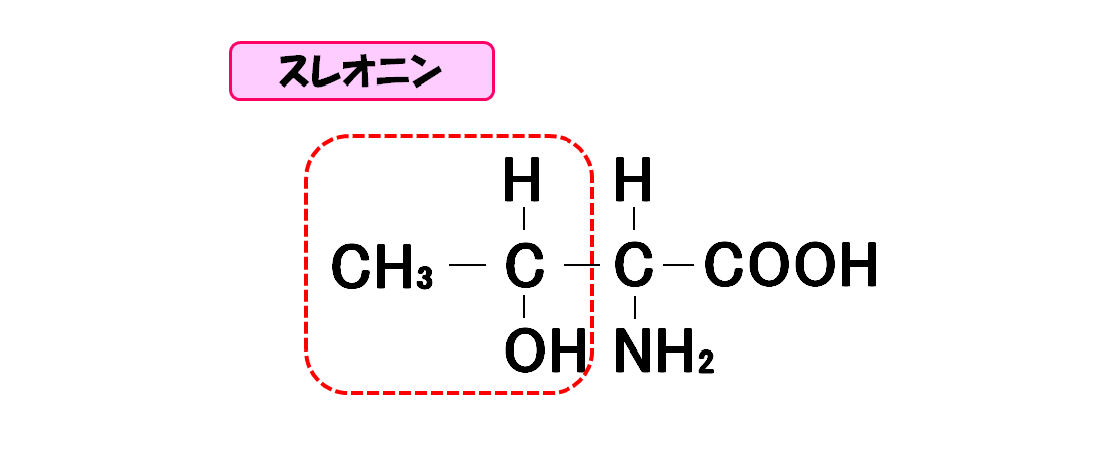
- 3文字略記号・・・Thr
- 1文字略記号・・・T
- 分子量・・・119.1
- 等電点・・・5.60
フェニルアラニン
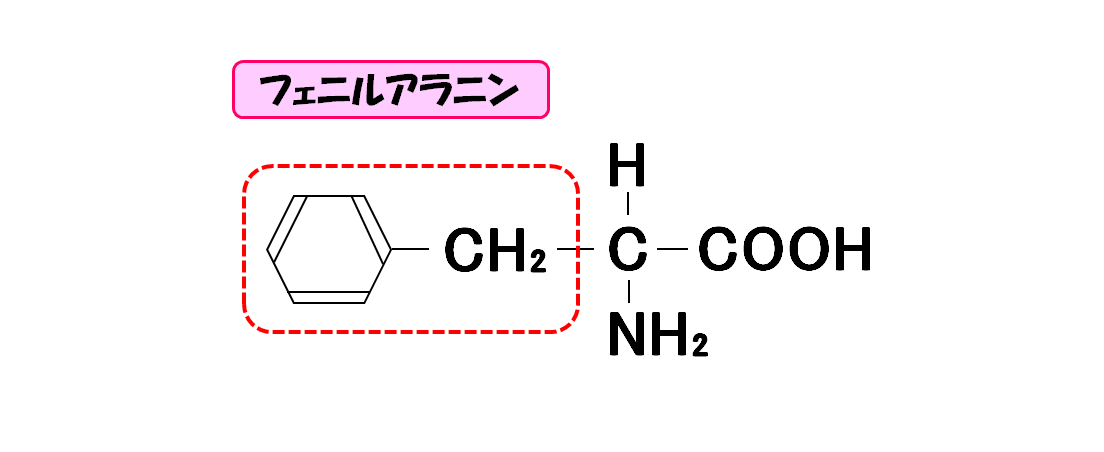
- 3文字略記号・・・Phe
- 1文字略記号・・・F
- 分子量・・・165.2
- 等電点・・・5.48
チロシン
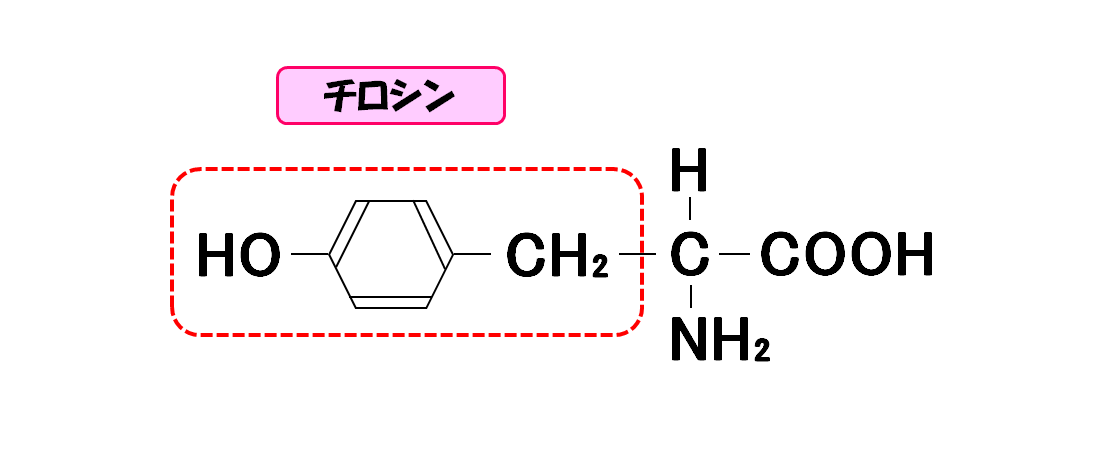
- 3文字略記号・・・Tyr
- 1文字略記号・・・Y
- 分子量・・・181.2
- 等電点・・・5.67
トリプトファン
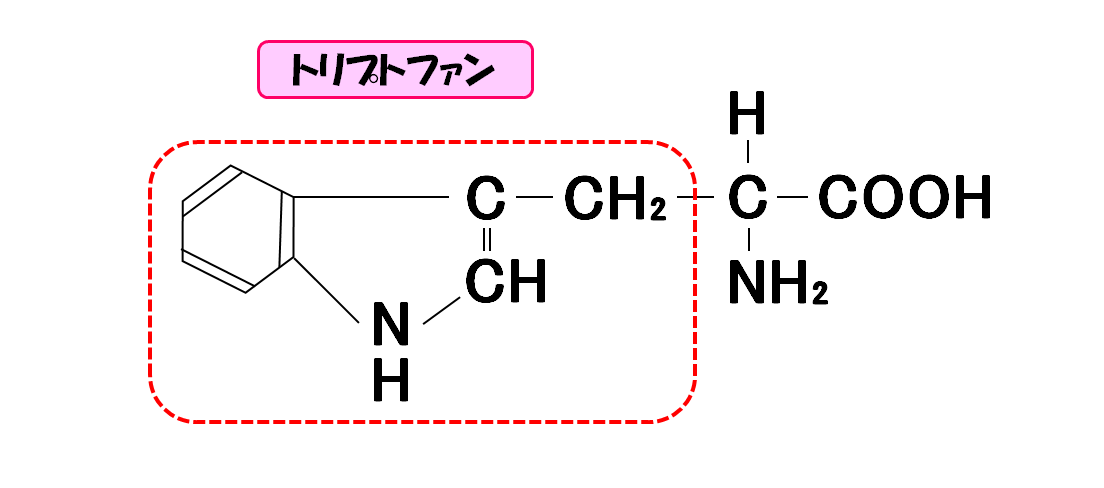
- 3文字略記号・・・Trp
- 1文字略記号・・・W
- 分子量・・・204.2
- 等電点・・・5.88
プロリン
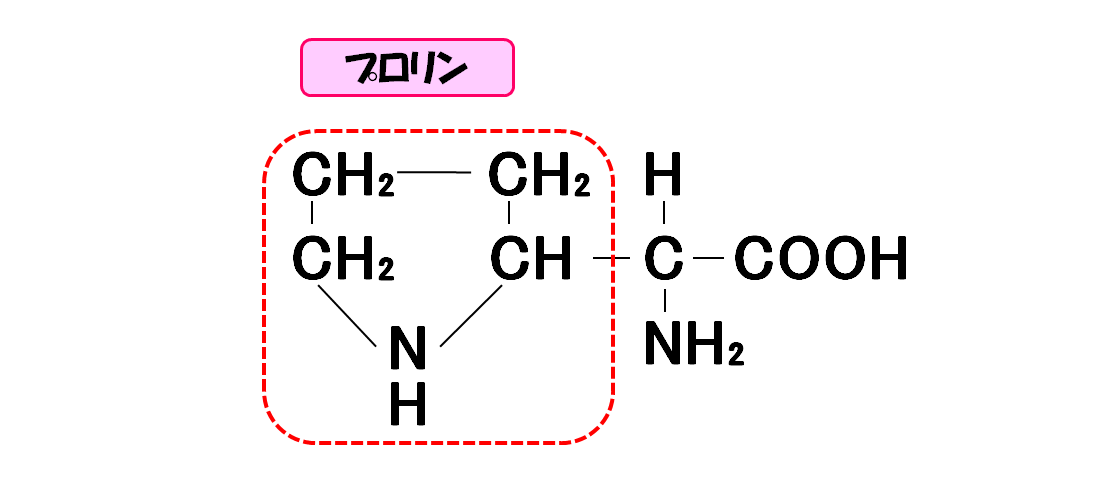
- 3文字略記号・・・Pro
- 1文字略記号・・・P
- 分子量・・・115.1
- 等電点・・・6.30
システイン
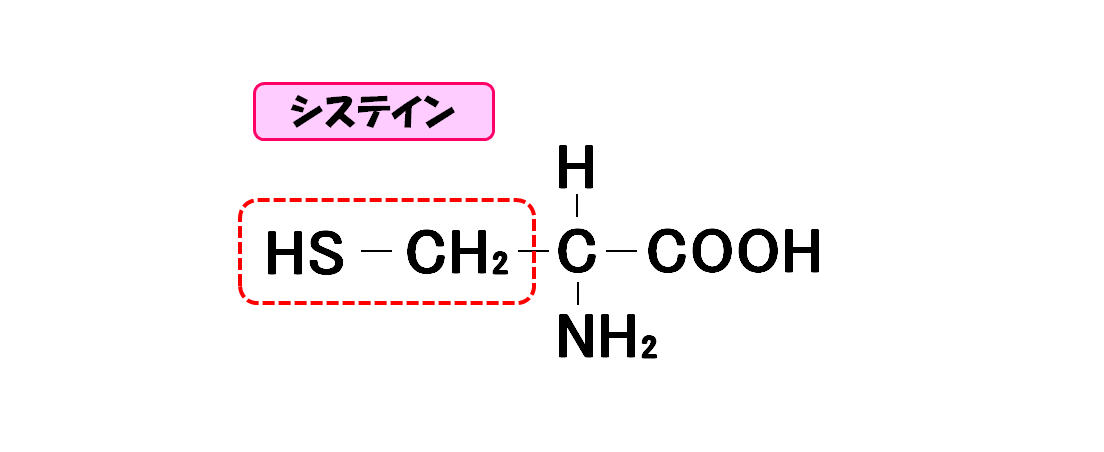
- 3文字略記号・・・Cys
- 1文字略記号・・・C
- 分子量・・・121.2
- 等電点・・・5.02
メチオニン
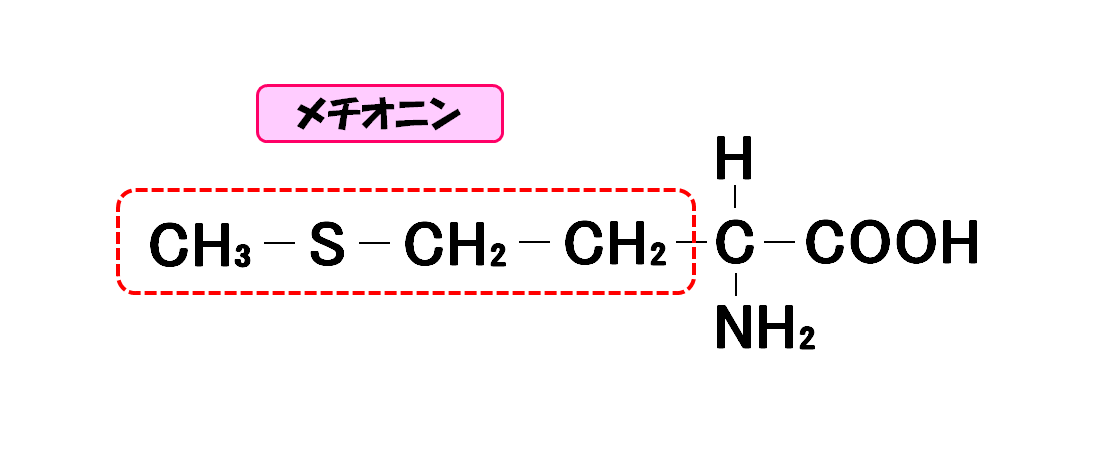
- 3文字略記号・・・Met
- 1文字略記号・・・M
- 分子量・・・149.2
- 等電点・・・5.06
アスパラギン
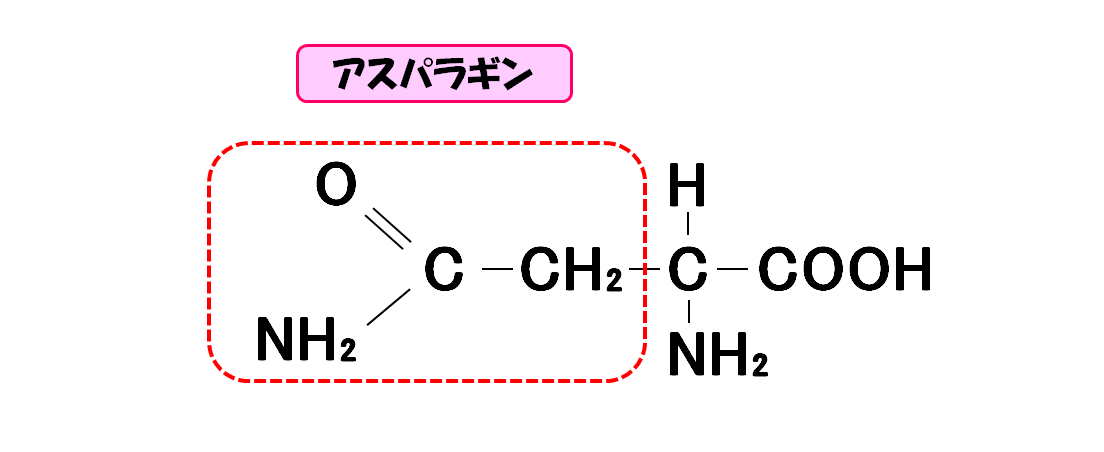
- 3文字略記号・・・Asn
- 1文字略記号・・・N
- 分子量・・・132.1
- 等電点・・・5.41
グルタミン
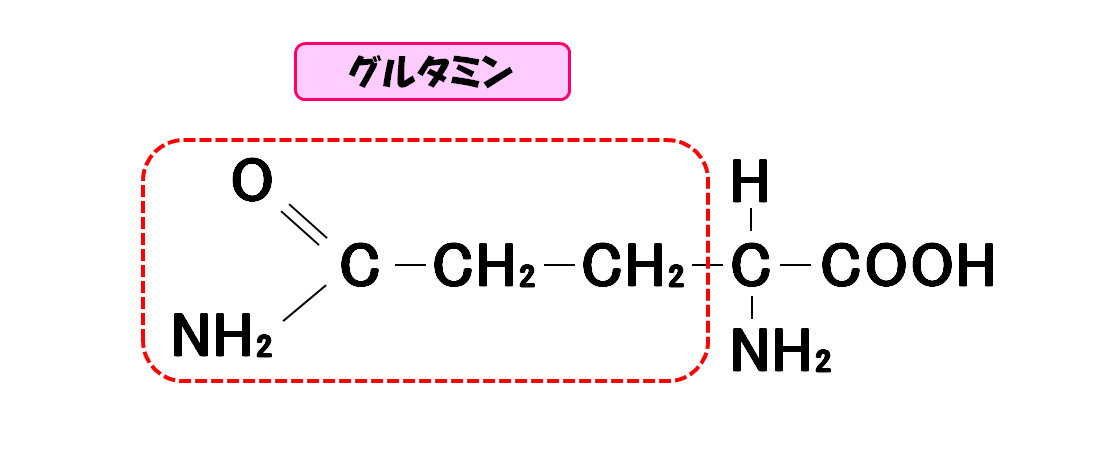
- 3文字略記号・・・Gln
- 1文字略記号・・・Q
- 分子量・・・146.2
- 等電点・・・5.70
アスパラギン酸
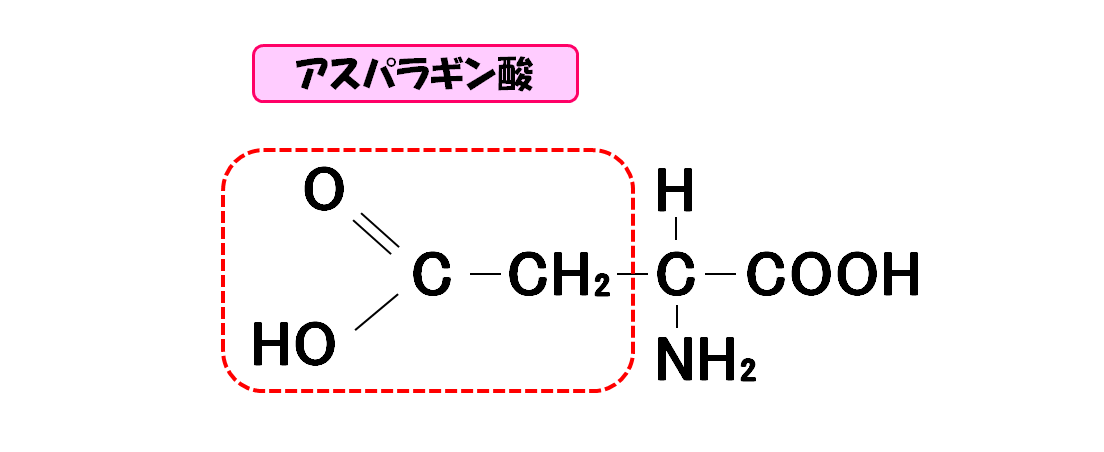
- 3文字略記号・・・Asp
- 1文字略記号・・・D
- 分子量・・・133.1
- 等電点・・・2.98
グルタミン酸
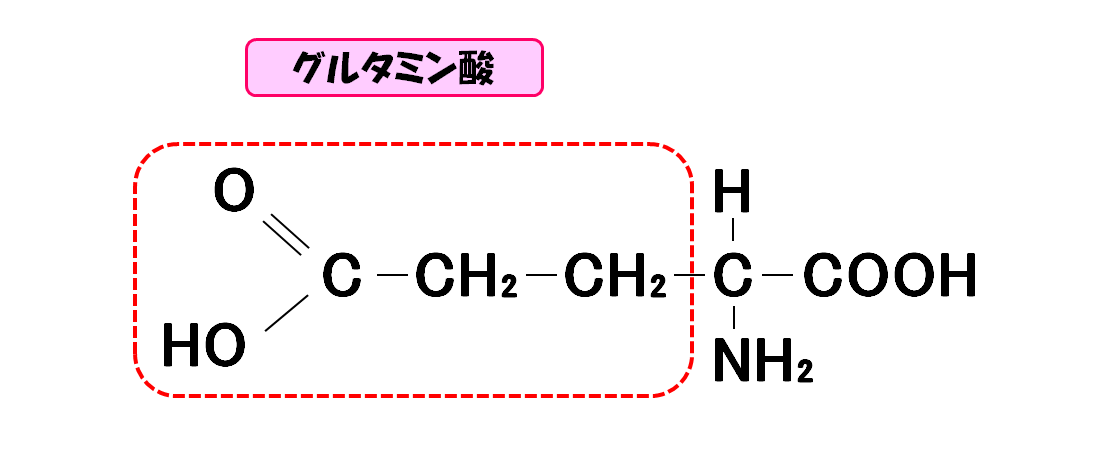
- 3文字略記号・・・Glu
- 1文字略記号・・・E
- 分子量・・・147.1
- 等電点・・・3.22
リジン
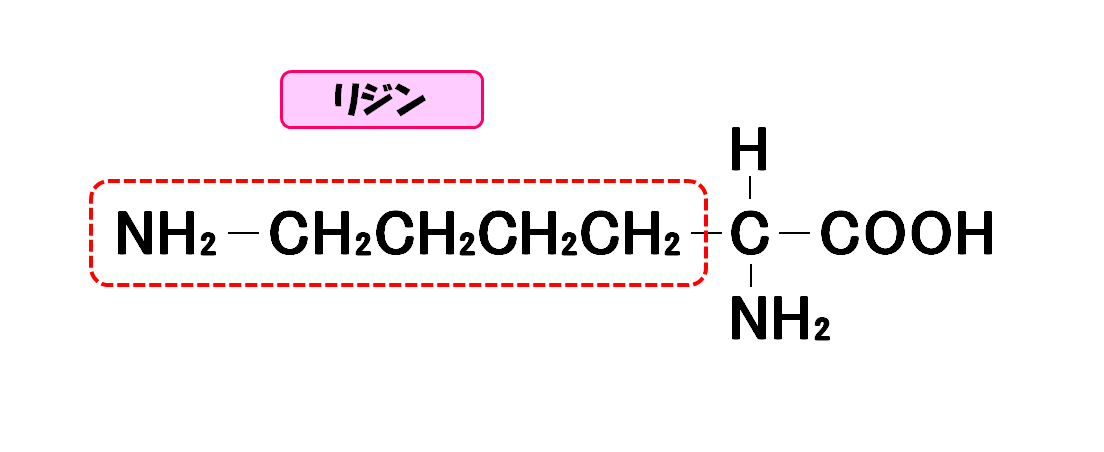
- 3文字略記号・・・Lys
- 1文字略記号・・・K
- 分子量・・・146.2
- 等電点・・・9.74
アルギン
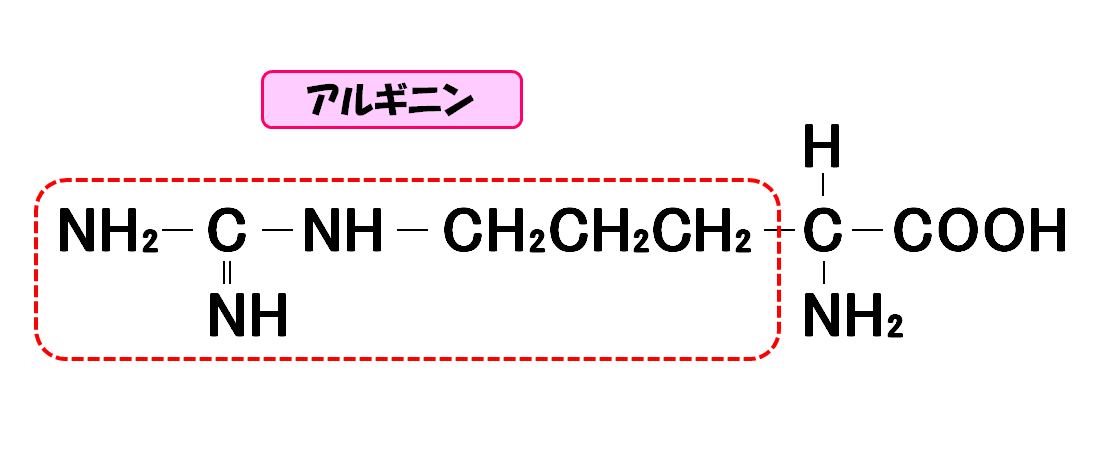
- 3文字略記号・・・Arg
- 1文字略記号・・・R
- 分子量・・・174.2
- 等電点・・・10.76
ヒスチジン
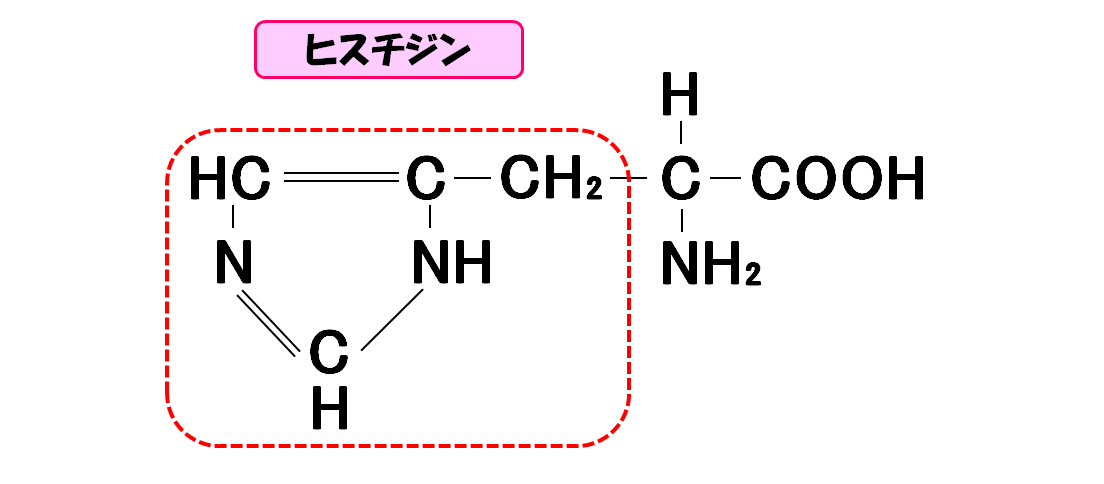
- 3文字略記号・・・His
- 1文字略記号・・・H
- 分子量・・・155.2
- 等電点・・・7.59
アミノ酸の特徴のまとめ
各アミノ酸の構造を見て納得したと思いますが、赤い部分以外は全て同じ形をしていましたね!
このように、たんぱく質はこれら20種類のアミノ酸が色々な割合で色々な配列をすることで、たくさんの種類が存在するのです。
20種類のアミノ酸についてまとめてますのでご覧ください!
| 分類 | 名称 | 3文字略 | 1文字略 | 分子量 | 等電点 | |
| 中性アミノ酸 | 脂肪族アミノ酸 | グリシン | Gly | G | 75.1 | 5.97 |
| アラニン | Ala | A | 89.1 | 6.02 | ||
| バリン | Val | V | 117.1 | 5.97 | ||
| ロイシン | Leu | L | 131.2 | 5.98 | ||
| イソロイシン | Ile | I | 131.2 | 6.02 | ||
| セリン | Ser | S | 105.1 | 6.68 | ||
| スレオニン | Thr | T | 119.1 | 5.60 | ||
| 芳香族アミノ酸 | フェニルアラニン | Phe | F | 165.2 | 5.48 | |
| チロシン | Tyr | Y | 181.2 | 5.67 | ||
| 複素環式アミノ酸 | トリプトファン | Trp | W | 204.2 | 5.88 | |
| プロリン | Pro | P | 115.1 | 6.30 | ||
| 含硫アミノ酸 | システイン | Cys | C | 121.2 | 5.02 | |
| メチオニン | Met | M | 149.2 | 5.06 | ||
| 酸性アミノ酸の 酸アミド |
アスパラギン | Asn | N | 132.1 | 5.41 | |
| グルタミン | Gln | Q | 146.2 | 5.70 | ||
| 酸性アミノ酸 | アスパラギン酸 | Asp | D | 133.1 | 2.98 | |
| グルタミン酸 | Glu | E | 147.1 | 3.22 | ||
| 塩基性アミノ酸 | リジン | Lys | K | 146.2 | 9.74 | |
| アルギン | Arg | R | 174.2 | 10.76 | ||
| ヒスチジン | His | H | 155.2 | 7.59 | ||
必須アミノ酸
天然のアミノ酸は約50種類ほど発見されています。
その中で食品のたんぱく質中には今紹介したアミノ酸20種類のみです。
この20種類のアミノ酸のうち、体内で合成されない、または十分に合成されないアミノ酸を必須アミノ酸と呼びます。
体内で作れないか作れてもその量が十分でないので、食品成分として外部からの摂取が必須になるアミノ酸なので必須アミノ酸と呼びます。
またはこの必須アミノ酸は不可欠アミノ酸とも呼ばれます。
この必須アミノ酸(不可欠アミノ酸)は20種類中9種類で、そのアミノ酸は以下の通りです。

- バリン
- ロイシン
- イソロイシン
- スレオニン
- メチオニン
- リジン
- ヒスチジン
- フェニルアラニン
- トリプトファン
以上9種類です。
これ以外のアミノ酸は他のアミノ酸から合成することが出来ます。
特に必須ではないため、非必須アミノ酸と呼んだりもします。
非必須アミノ酸は11種類ですね!

このうちシステインとチロシンは、それぞれメチオニンとフェニルアラニンから体内で合成することが出来ます。
そのため、食品成分表のアミノ酸組成表ではメチオニンとシステインを合わせて含硫アミノ酸、フェニルアラニンとチロシンを合わせて芳香族アミノ酸と表示しています。
まとめ
今回はたんぱく質を構成するアミノ酸について解説してきました!
それでは簡単に復習したいと思います!
- たんぱく質の最小単位はアミノ酸である
- アミノ酸は炭素(C)を中心にアミノ基(-NH₂)、カルボキシル基(-COOH)、水素(H)、側鎖(R)がそれぞれ結合している
- 側鎖(R)の違いにってアミノ酸の種類や特徴が変わる
- たんぱく質を構成するアミノ酸は20種類ある
- 人間が体内で合成できない、または合成できてもその量が十分でないので外部からの摂取が必須とされるアミノ酸が9種類ある
- 必須アミノ酸は①バリン②ロイシン③イソロイシン④スレオニン⑤メチオニン⑥リジン⑦ヒスチジン⑧フェニルアラニン⑨トリプトファンである。
いかがでしたか?
それではまた次回の記事も是非楽しみにしていてください!











