【優しすぎる解説】たんぱく質の構造についてまとめてみた!

こんにちは!
私は平成生まれの管理栄養士です!
前回はたんぱく質を構成するアミノ酸について、その種類や構造、特性などについて解説してきました。
今回はたんぱく質の構造についてです。
これまでの記事では、たんぱく質の構造はほんとうにアバウトに大切なポイントのみを紹介してきましたが、今回は少しだけ詳しく解説したいと思います。
それでは早速見ていきましょう!
たんぱく質を構成する20種類のアミノ酸
たんぱく質の構造を知るうえでは、アミノ酸について最低限知っておかないといけません。
たんぱく質を細かく分解していくと、最終的にはアミノ酸になります。
そして、たんぱく質を構成しているアミノ酸はたった20種類しかありません。
人の体内に存在するたんぱく質も、食品中に含まれているたんぱく質も、それを構成するアミノ酸の種類は20種類です!
どのようなアミノ酸があるのでしょうか?
たんぱく質の構成する20種類のアミノ酸は以下の通りです。
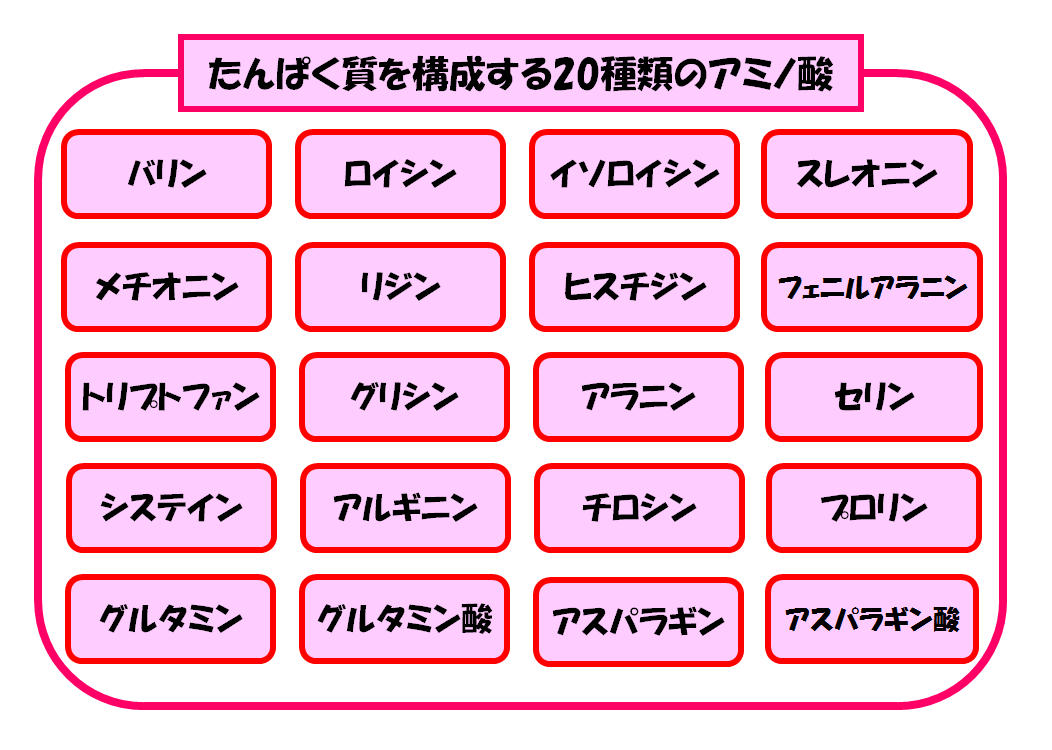
この20種類のアミノ酸の中で、体内で作ることができない、もしくは作れるがその量が十分でないアミノ酸を必須アミノ酸(不可欠アミノ酸)と呼びます。
この必須アミノ酸は9種類です。
一方で必須アミノ酸ではなく、体内で合成可能なアミノ酸のことを非必須アミノ酸と言います。
それぞれどういったアミノ酸があるのかについては下の図にまとめてあります!
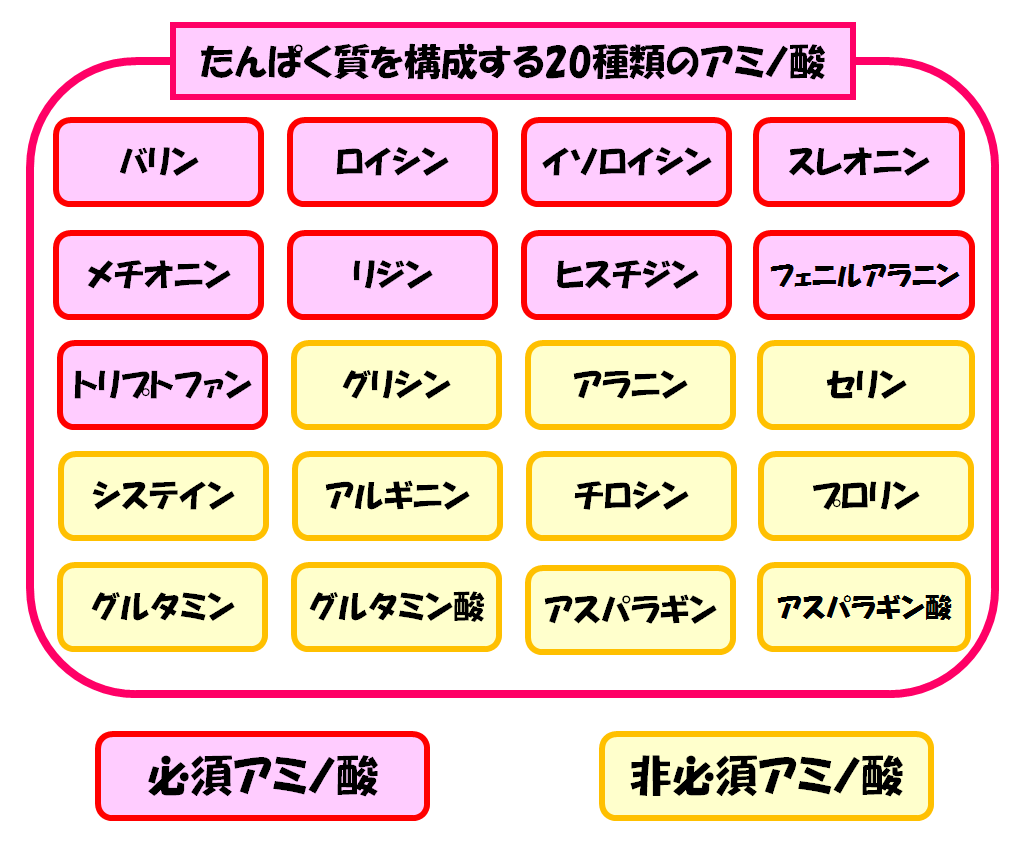
これらの20種類のアミノ酸がつながってたんぱく質を構成しているのです。
おおまかなたんぱく質の構造
まずはたんぱく質の構造をまずおおまかに理解すると良いと思います。
ここでは簡単にたんぱく質の構造を説明します!
たんぱく質は主に次の4つの構造になっています。
- 一次構造
- 二次構造
- 三次構造
- 四次構造
一次構造は、アミノ酸同士がつながって一本の鎖になった状態です。
こうしてたくさんのアミノ酸がくっついたものをポリペプチドど呼びます。
二次構造では、一次構造によってできたアミノ酸が特徴的な形をとっています。
アミノ酸の一本の鎖は直鎖状に伸びるわけではなく、二次構造によっていくつかの特徴的な形になるのです。
三次構造では、ポリペプチドがさらに折れ曲がったり畳まれたりして一定の複雑な立体構造をとります。
ここまでくると、たんぱく質としての機能をもつものもでてきます。
一本のアミノ酸の鎖でできているのはこの三次構造までです。
四次構造では、三次構造をとったたんぱく質がさらにいくつか集まって集合体になったものです。
このようにたんぱく質の構造は一~四次構造と大きく4つの構造に分けることができるのです。
それぞれの構造のイメージ図を下にまとめてありますのでご覧ください!
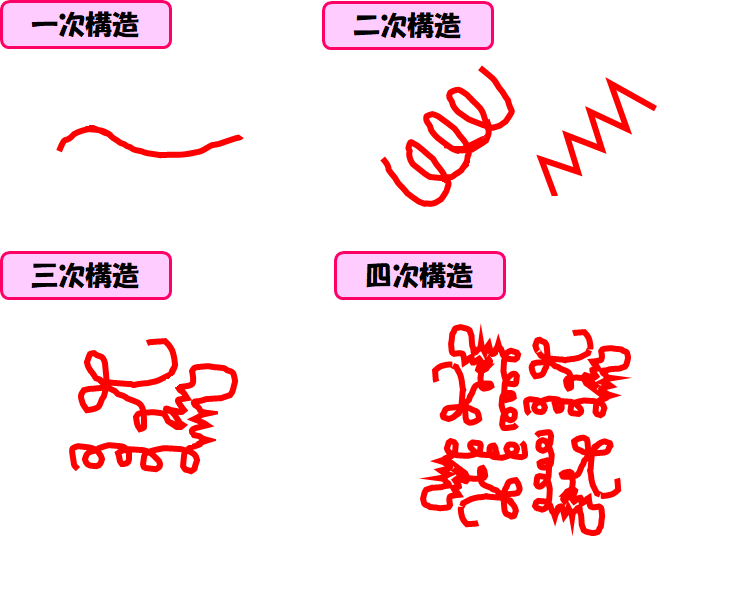
それでは、おおまかなたんぱく質の構造が分かったところでそれぞれ少し詳しく見ていきましょう!
一次構造

たんぱく質の一次構造のイメージとしてはネックレスです!
たんぱく質の一番最初の構造は、アミノ酸がネックレスのようにつながっているようなものです。
一次構造のアミノ酸の鎖をもう少し拡大すると、このようになります。
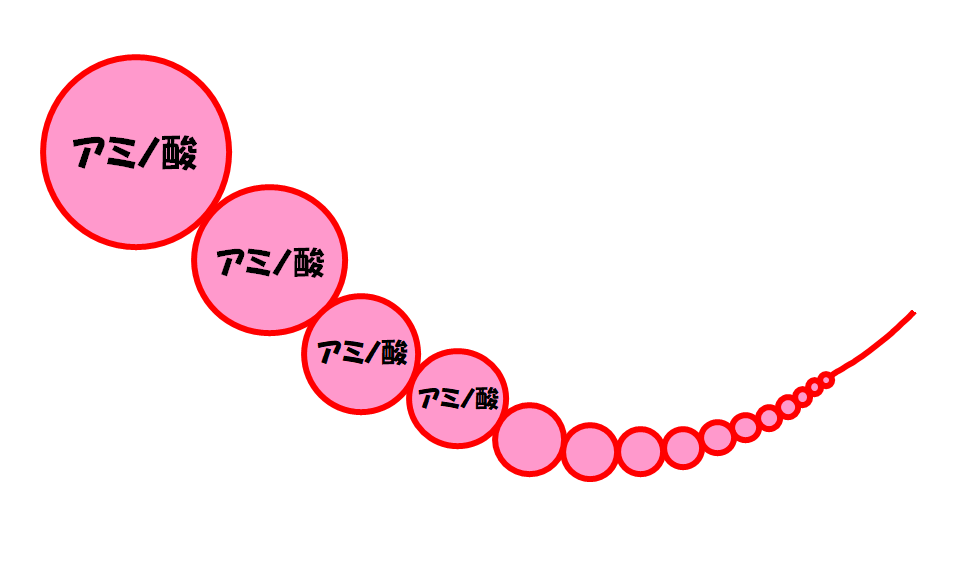
このようにアミノ酸同士が永遠とネックレスのようにつながっているのが一次構造です。
このアミノ酸同士の結合には特徴があります。
アミノ酸のカルボキシル基(-COOH)と隣のアミノ酸のアミノ基(-NH₂)が結合します。
この結合をペプチド結合と言います。
たんぱく質を構成するアミノ酸は20種類ありますが、全てのアミノ酸にはこのカルボキシル基(-COOH)と、アミノ基(-NH₂)があります。
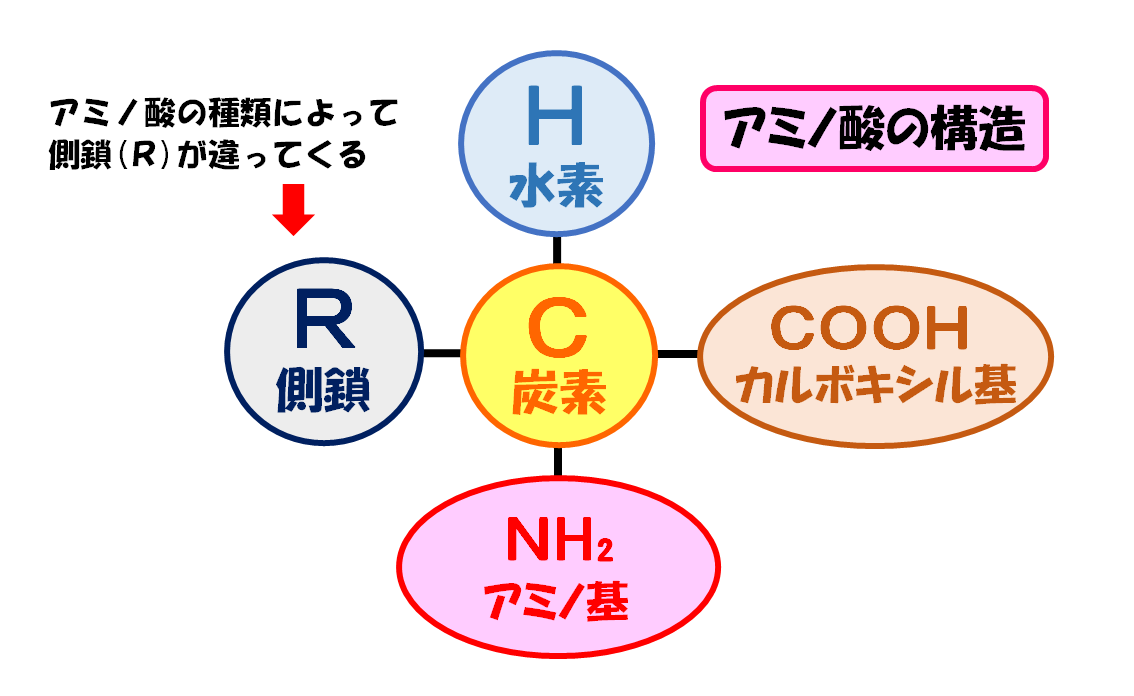
このように全てのアミノ酸にカルボキシル基(-COOH)とアミノ基(-NH₂)があるので、アミノ酸同士がペプチド結合し一本のアミノ酸の鎖ができるのです。
アミノ酸同士のペプチド結合を詳しく見ると、このようになっています。
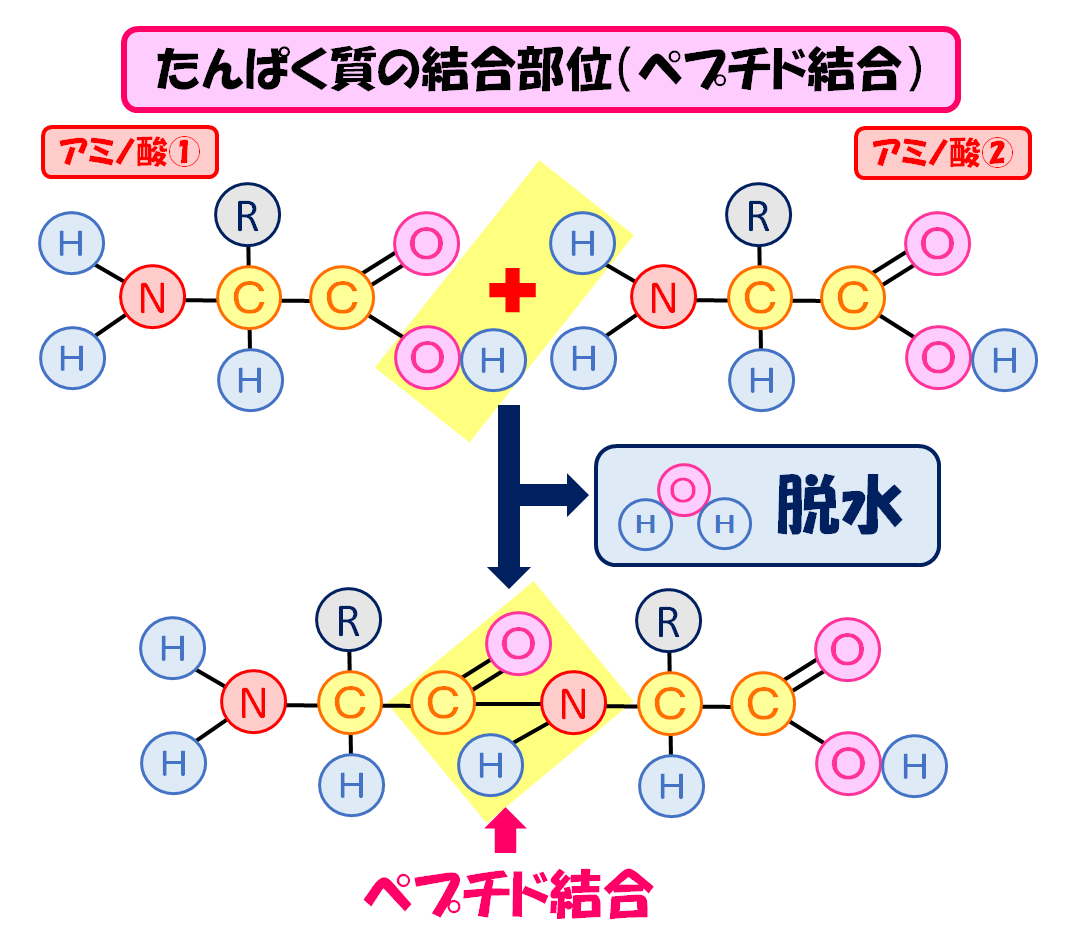
図を見てもわかるように、アミノ酸同士の結合では水が抜けます。(脱水)
ペプチド結合はたんぱく質の構造において最も基本的な構造と言えます。
アミノ酸が2つ結合したものをジペプチド、たくさん結合したものをポリペプチドといいます。
こうしてたくさんのアミノ酸がペプチド結合をすることで一本の鎖ができます。
このアミノ酸の結合でできた鎖をペプチド鎖と呼んだりもします。
この一次構造でのアミノ酸の配列がどのようになるのかで、そのたんぱく質の特徴や種類が変わってくるのです。
二次構造

一次構造でできたペプチド鎖はずっと真っ直ぐ伸びていくわけではありません。
ある決まった形をとっているのです。
アミノ酸同士のペプチド結合が長くなると、アミノ酸同士の相互作用によってらせん状の規則的な構造を作ります。
このらせん構造をα-ヘリックスと呼びます。
また、ジグザグに伸びたペプチド鎖2本が平行、または逆平行に並んで向かい合ってシート状の構造になります。
このシート型の構造をβ-シートと呼びます。
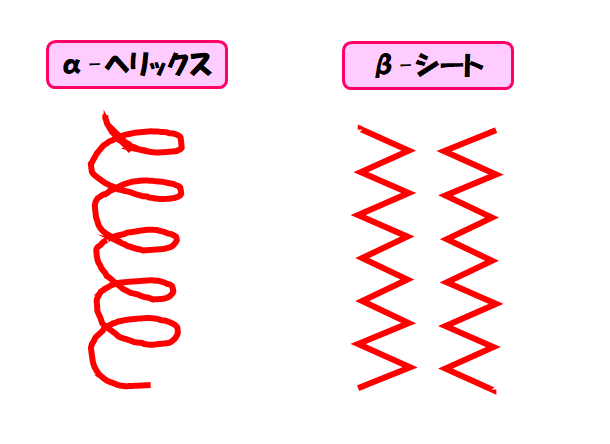
三次構造

二次構造である一定の構造をとったペプチド鎖はさらに折れ曲がったり畳まれたりします。
こうすることで、たんぱく質は立体構造をとるのです。
この立体構造はその種類によって球状や繊維状になります。
このような立体構造を三次構造と呼びます。
三次構造で立体的になるには、様々なタイプの結合が関わってきます。
S-S結合、水素結合、イオン結合、疎水結合などです。
このようなそれぞれの結合が作用して、たんぱく質は立体構造になりたんぱく質としての生理活性をもちます。
イメージしにくいと思うので図に様々な結合をまとめてあります!
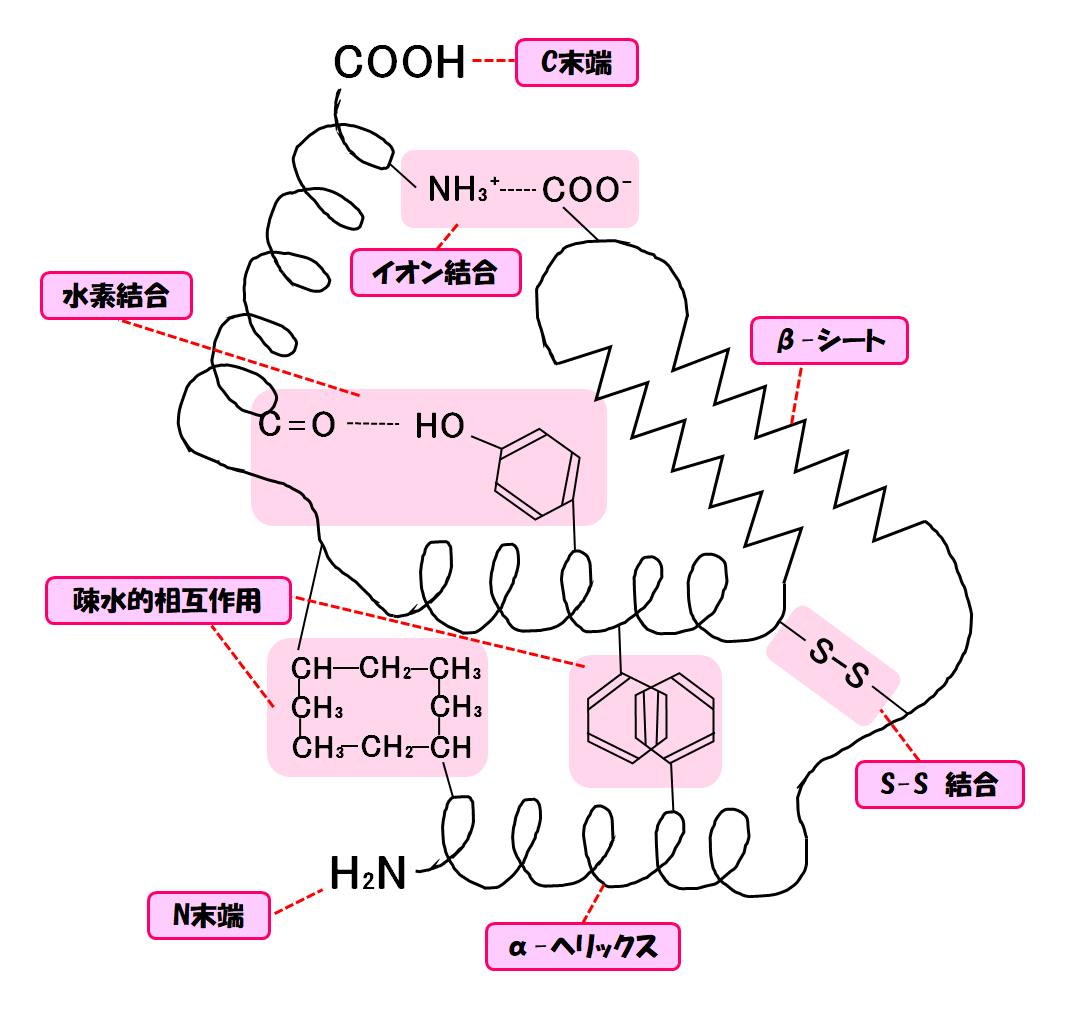
こうして一次構造、二次構造、三次構造により、それぞれのたんぱく質固有の立体構造を形成して様々な機能を発揮することが出来るのです。
四次構造

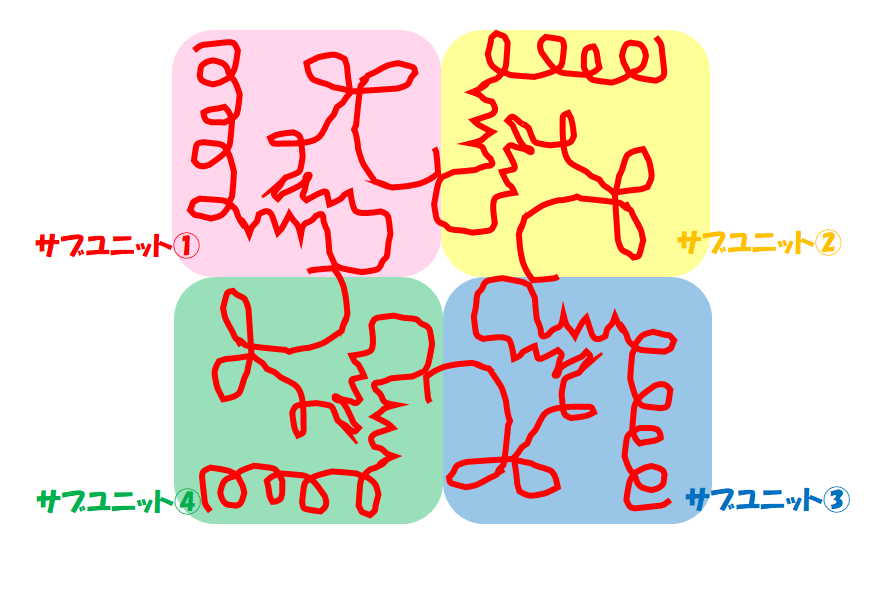
四次構造とは三次構造をもつたんぱく質が複数個集まってできた空間的構造のことです。
いくつかのユニットが集まって1つの集団として新しい機能を持つようになります。
その三次構造を持つ一つ一つのペプチド鎖をサブユニットと呼びます。
このようなサブユニットが集まっている四次構造は、赤血球に含まれるヘモグロビンや酵素などにみられます。
これまで紹介してきた構造の中で、二次構造、三次構造、四次構造は高次構造と言います。
これらは物理的または化学的要因の刺激によって、高次構造が破壊されて生理活性が失われます。
この生理活性が失われることを専門的には変性と言います。
このたんぱく質の変性に関与する物理的・化学的要因の刺激をいくつか紹介します。
- 加熱
- 凍結
- 乾燥
- 撹拌
- 電磁波
- 酸
- アルカリ
- 有機溶媒
- 重金属
たんぱく質を変性させる要因はこのようなものがあるのです。
まとめ
いかがでしたか?
たんぱく質の構造について解説してきましたが最後に簡単にまとめたいと思います。
- 一次構造・・・アミノ酸同士がペプチド結合を繰り返した一本のペプチド鎖
- 二次構造・・・ペプチド鎖がある一定の規則的な形をとる ①α-ヘリックス ②β-シート
- 三次構造・・・二次構造のペプチド鎖がさらに折れたり、畳まれたりして球状や繊維状の形をつくる
- 三次構造に関与する結合には ①S-S結合 ②水素結合 ③イオン結合 ④疎水結合 などがある
- 四次構造・・・三次構造をもつサブユニットが複数個集まって空間的構造をとる
以上です!
次回も楽しみにしていてください!











